Harapan
masyarakat mendapatkan obat Covid-19 yang benar-benar tepat masih harus
menunggu tahapan uji klinis selesai. Sementara Badan Pengawasan Obat dan
Makanan (BPOM) masih memberikan koreksi pada hasil uji klinis tim peneliti
Universitas Airlangga (Unair) bersama Badan Intelejen Negara (BIN) dan TNI AD.
Lalu setelah koreksi selesai dilakukan, kapan obat tersebut akan bisa diproduksi
massal dan diedarkan?
Dalam
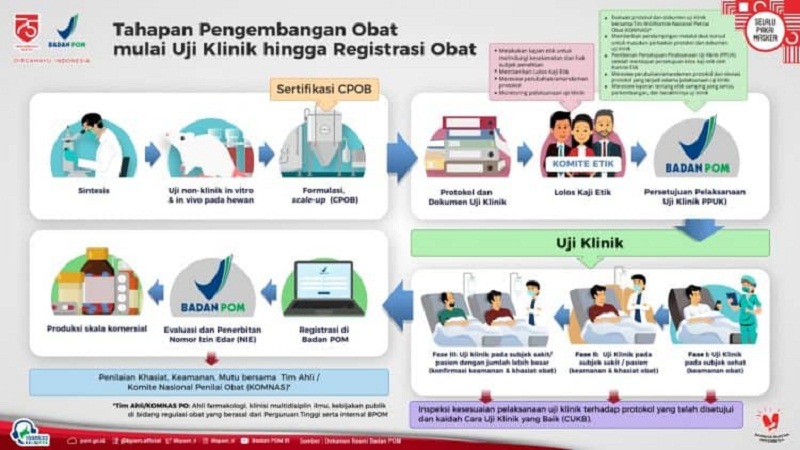
data BPOM, alur tahapan pengembangan obat dari mulai uji klinis hingga registrasi
obat siap edar di antaranya,
Uji
Non-Klinis pada Hewan
Percobaan
sintesis dilakukan lalu diteruskan dengan uji non klinis in vitro dan in vivo
pada hewan.
Persetujuan
Uji Klinis
Peneliti
menyusun protokol dan dokumen uji klinis. Lalu mengikuti kajian etik.
Selanjutnya BPOM mengeluarkan Persetujuan Pelaksanaan Uji Klinis.
Uji
Klinis Fase I, II, III
Fase
I dilakukan pada pasien sehat.
Fase
II dilakukan pada subjek sakit, khasiat dan keamanan obat.
Fase
III dilakukan pada pasien sakit dalam jumlah yang lebih besar.
Selanjutnya
BPOM melakukan inspeksi kesesuaian pelaksanaan uji klinis terhadap protokol
yang telah disetujui dan kaidah Cara Uji Klinis yang Baik (CUKB).
Persetujuan
BPOM
Jika
lolos dan disetujui BPOM, maka obat bisa teregistrasi di BPOM.
Izin
Edar
Setelah
itu BPOM melakukan evaluasi dan Penerbitan Nomor Izin Edar (NIE)
Obat
Diedarkan
Setelah
itu, obat bisa diproduksi skala komersial.
Terkait
semua tahapan itu, Kepala BPOM Penny Lukito menjelaskan tugas BPOM adalah
melindungi masyarakat memastikan temuan obat yang valid dan aman. Komitmen
BPOM, kata dia, memberikan perlindungan dan juga memastikan proses uji klinis
riset dari setiap obat dan vaksin berlangsung dengan tata cara kaidah
scientific yg sesuai dengan standar berlaku secara internasional.
“BPOM
selama ini juga memiliki kredibilitas yang baik di mata internasional. Kalau
nanti hasilnya (koreksi) dianggap selesai, hasil koreksi sudah diperbaiki dan
dianggap valid, maka kami bisa berikan kebijakan emergency untuk segera menerbitkan
izin edar,†jelasnya.
Berapa
lama prosesnya?
“Setelah
disetujui, maka prosesnya membutuhkan 20 hari kerja. Tapi tentunya menuju
proses 20 hari kerja itu kami tentu akan dibantu oleh tim Komnas Penilai Obat.
Tapi sampai ke tahap itu (izin edar), uji klinis harus berjalan dengan baik.
Baru setelah itu bisa diserahkan ke kami, agar diproses izin edar. (Untuk saat
ini obat Unair), belum sampai ke sana (izin edar),†tegasnya. (*)